Legame ammidico
Formazione del legame ammidico
Il legame ammidico è il legame chimico che unisce il gruppo carbossilico R'-COOH e il gruppo amminico R2-NH di due composti diversi.
Nella formazione del legame ammidico il gruppo -COOH di una molecola condensa con il gruppo amminico dell'altra molecola.
Viene liberata una molecola di H2O e si forma il legame ammidico R'-CO-NR2.
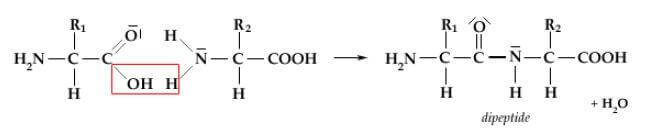
Il meccanismo di formazione del legame ammidico può essere rappresentato come nello schema di seguito proposto:

Il legame ammidico è il tipico legame presente nelle proteine; in questo caso prende il nome specifico di legame peptidico. Il composto che si ottiene quando due amminoacidi condensano tra loro prende il nome di dipeptide.
Tautomeria nel legame ammidico
Il legame ammidico non ha le proprietà di un singolo legame ma per il 40% ha le proprietà tipiche di un doppio legame e per il 60% ha le proprietà tipiche di un singolo legame.
Ciò è dovuto ad una forma di tautomeria (simile per molti aspetti alla tautomeria cheto-enolica) che coinvolge il gruppo ammidico.

In seguito a questo fenomeno non è permessa la libera rotazione attorno al legame C-N.
Conformazione trans del legame ammidico
Nel legame ammidico l'ossigeno del gruppo carbonilico e l'eventuale idrogeno del gruppo amminico sono generalmente disposti in conformazione trans.

Questa conformazione non è casuale ma dipende dal minor ingombro sterico delle catene laterali.
Studia con noi