Addizione al doppio legame C=C
Reazioni di addizione al doppio legame carbonio-carbonio
La chimica degli alcheni è in buona parte la chimica del doppio legame carbonio-carbonio. Il doppio legame consiste di un legame σ forte e di un legame π debole.
I tipi di reazione che ci possiamo attendere dagli alcheni sono quelli in cui viene rotto il legame π e vengono formati due nuovi legami σ forti.
Una reazione di questo genere è chiamata reazione di addizione al doppio legame carbonio-carbonio e può essere così schematizzata:

In una reazione di addizione una molecola insatura e un altro reagente si combinano insieme per dare un unico prodotto saturo.
La molecola ottenuta contiene due nuovi legami σ mentre le molecole reagenti contenevano un legame π (l'alchene) e un legame σ (il reagente X―Y).
Avendo il legame π proprietà elettron-donatrici (base di Lewis), ci si può aspettare che dei reattivi che cercano elettroni (reattivi elettrofili o acidi di Lewis) si addizioneranno facilmente al doppio legame di un alchene: proprio per tale motivo l'addizione caratteristica degli alcheni è l'addizione elettrofila.
La reazione di addizione elettrofila si svolge in due tappe ben distinte:

Nella prima tappa (stadio lento della reazione) si ha l'addizione all'alchene del componente "positivo" dell'addendo con formazione di un carbocatione:
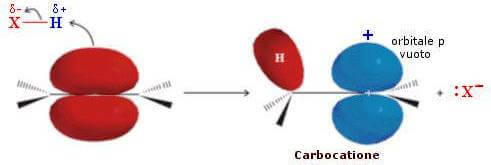
Nella seconda tappa (stadio veloce della reazione) si ha un attacco nucleofilo del componente negativo dell'addendo (:X−).
L'attacco può avvenire verso entrambi i lobi dell'orbitale p vuoto del carbocatione:
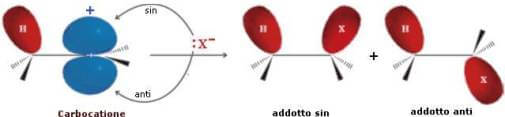
Al contrario, i reagenti elettron-donatori nucleofili sono poco o niente reattivi nei confronti del doppio legame, a meno che non siano presenti nell'olefina dei sostituenti a forte potere elettron-attrattore.
Un esempio di reazione che svolge attraverso questo meccanismo è l'addizione di acidi alogenidrici al doppio legame C=C di un alchene.
Studia con noi