Condensazione
Passaggi di stato: la condensazione
La condensazione è il passaggio di una sostanza dallo stato di vapore allo stato liquido; è il passaggio inverso dell'evaporazione; si tratta quindi di un passaggio di stato che avviene per sottrazione di calore ad opera di una sorgente esterna.
Affinché la condensazione possa avvenire, è necessario che il vapore sia saturo, ovvero che sia in equilibrio con il proprio liquido; un vapore surriscaldato, ad esempio, può condensarsi solo dopo aver raggiunto, tramite raffreddamento, questa condizione.

I passaggi di stato della materia: la condensazione corrisponde al passaggio → vapore liquido.
Il valore della pressione di un vapore saturo è nota come tensione di vapore ed è il valore della pressione a cui avviene il passaggio di stato: essa è una grandezza fisica che dipende della sola temperatura.
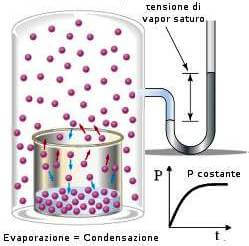
La pressione gassosa corrispondente all'equilibrio liquido-vapore viene indicata come tensione di vapor saturo. Il suo valore dipende dalla temperatura.
La condensazione da un punto di vista microscopico
Raffreddando i vapori di una sostanza, l'energia cinetica media delle sue particelle diminuisce, con il che ad un certo punto le loro mutue forze di coesione prevalgono, e la sostanza inizia a passare allo stato liquido.
Durante il processo della liquefazione la temperatura rimane costante, in quanto il calore che viene sottratto dal sistema è quello che viene liberato nella formazione del legame fra le particelle allo stato liquido (energia di legame).
Quindi, ad esempio, sottraendo calore e quindi condensando del vapore acqueo alla pressione di 1 atm, per tutta la durata del processo e sino a quando l'ultima piccola frazione di vapore non è condensata, la temperatura rimane costante a 100°C. Solo una volta ultimata la condensazione, continuando a sottrarre calore al sistema, la temperatura dell'acqua allo stato liquido inizia a calare.
Il calore sottratto durante la condensazione viene detto "latente" e corrisponde, come detto in precedenza, al calore che viene liberato nella formazione del legame fra le particelle che passano allo stato liquido.
Mentre un vapore puro condensa ad una determinata temperatura che rimane costante per tutto il processo, le miscele di vapori condensano in un intervallo di temperature: si separano prima i componenti meno volatili, quindi i più volatili. Tale fenomeno è sfruttato nella condensazione frazionata per separare i componenti della miscela di vapori.
Influenza della pressione sulla temperatura di condensazione
La temperatura di condensazione di una sostanza (come ad esempio l'acqua) dipende dalla pressione ; più in particolare all'aumentare della pressione che grava sul sistema, la temperatura di condensazione aumenta.
È per questo motivo che in alta montagna dove l'aria è più rarefatta e la pressione atmosferica è minore, l'acqua condensa ad una temperatura inferiore ai 100°C.
Differenza tra condensazione e liquefazione
La condensazione non è da confondere con la liquefazione che è il passaggio dallo stato gassoso allo stato liquido e che avviene solo a determinate pressioni e temperature. Quindi, se abbiamo del vapore acqueo diremo che il vapore condensa, mentre se avremo dell'azoto, che a differenza del vapore acque è un gas e non un vapore, diremo che liquefa.
Pertanto,
1) condensazione: vapore → liquido
2) liquefazione: gas → liquido
Ricordiamo infine che gas e vapori sono entrambi aeriformi con la differenza che i vapori possono essere condensati per sola compressione.
Calore latente di condensazione
Il calore latente di condensazione è la quantità di energia liberata da 1 g di sostanza in fase di condensazione. Nel Sistema Internazionale si misura in J/kg. È una proprietà intensiva della materia e caratteristica per ogni sostanza pura.
Il calore latente di condensazione è numericamente uguale ma di segno opposto al calore latente di vaporizzazione. Il calore latente di condensazione del vapore acqueo corrisponde a - 2260 j/g = -540 cal/g.
Temperature di condensazione di alcune sostanze
Ogni vapore ha una sua temperatura di condensazione esattamente definita. Di seguito riportiamo le temperature di condensazione di alcune importanti sostanze determinate alla pressione di 1 atm:
Mercurio = - 39°C
Alcol etilico = 78,5 °C
Acqua = 100°C
Zolfo = 115°C
Sodio = 900°C
Sale da cucina = 1465 °C
Link correlati:
Quanto vale il calore latente dell'acqua?
Che cos'è la curva di riscaldamento di una sostanza pura?
Che cos'è la curva di raffreddamento di una sostanza pura?
Studia con noi