Modelli atomici
Quali sono i modelli atomici?
Vuoi sapere quali sono i princpali modelli atomici?
Vuoi conoscere cosa affermano i principlai modelli atomici?
Se si continua con la lettura dell'articolo.
Iniziamo col dire che, in chimica, i modelli atomici sono un insieme di teorie che cercano di descrivere la struttura atomica.
I modelli atomici si propongono quindi di spiegare la struttura e il funzionamento degli atomi.
Di seguito vengo descritti i principali modelli atomici che si sono susseguiti nel corso della storia.
Modello atomico di Dalton
Il primo modello atomico basato su dati sperimentali è quello di J. Dalton. Nel 1803 il fisico inglese, analizzò la legge di Lavoisier e la legge di Proust, incrociando i dati ottenuti da questi scienziati con quanto espresso nella legge da lui stesso enunciata nota oggi come legge di Dalton.
Egli intuì che solo immaginando la materia costituita da atomi piccolissimi, indivisibili, indistruttibili e non creabili, si potevano spiegare le tre leggi sopra indicate e formulò quello che oggi è noto come il modello atomico di Dalton.
Per ulteriori info si veda: modello atomico di Dalton.
Modello atomico di Thomson
In seguito alla scoperta di cariche positive e cariche negative costituenti la materia, nel 1904, il fisico inglese J.J. Thomson formulò il proprio modello atomico secondo il quale gli elettroni (di carica negativa) sono dispersi come gli acini di uvetta in un panettone (da qui il nome di "modello atomico a panettone") in una massa elettricamente positiva, in modo da determinarne l'equilibrio delle cariche. Tale modello atomico prende il nome di modello atomico di Thomson.
Modello atomico di Rutherford
Nel 1911 lo scienziato neozelandese E. Rutherford bombardò una sottilissima lamina di oro con raggi alfa.
Poiché le particelle alfa nella maggior parte dei casi oltrepassavano la lamina d'oro senza subire deviazioni, significava che non incontravano alcun ostacolo sul proprio cammino e che quindi, l'atomo doveva essere formato prevalentemente da spazio vuoto. Tale modello atomico prende il nome di modello atomico di Rutherford.
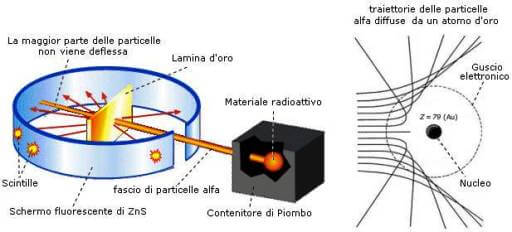
Rappresentazione dell'esperimento di Rutherford.
Modello atomico di Bohr
Nel 1913 gli studi sugli spettri di emissione e sugli spettri di assorbimento dell'idrogeno e di altre sostanze, indussero il fisico danese N. Bohr a pensare che gli elettroni si muovessero nello spazio soltanto in orbite circolari di ben definita energia (orbite stazionarie o livelli di energia).
Tale modello atomico prende il nome di modello atomico di Bohr.
Modello a orbitali
Secondo tale modello atomico gli elettroni si muovono entro zone che circondano il nucleo note come orbitali.
Racchiudendo entro una superficie limitante tutti i punti per i quali l'elettrone ha la massima probabilità di passare nel suo moto intorno al nucleo, si ottiene una figura geometrica, simmetrica rispetto al nucleo, che dà un idea della "forma" dell'orbitale. Esistono diversi tipi di orbitali: orbitale s, orbitale p, orbitale d e orbitale f sono i più importanti.
Tale modello atomico prende il nome di modello atomico a orbitali.
Link correlati:
Che cos'è la meccanica razionale?
Qual è la differenza tra orbita e orbitale?
Come si scrive una configurazione elettronica?
Studia con noi