Saggi alla perla al borace
Relazione di laboratorio: saggi alla perla al borace
Introduzione
Per riscaldamento alla fiamma, il borace (tetraborato di sodio decaidrato Na2B4O7· 10H2O) perde l'acqua di cristallizzazione e si trasforma in una massa fusa vetrosa (perla) di metaborato di sodio e anidride borica (NaBO2 · B2O3) che può essere utilizzata per saggiare alla fiamma alcuni composti i cui cationi metallici colorano la perla in modo caratteristico.
Scopo dell'esperienza
Identificare alcuni metalli in base al colore che impartiscono alla perla al borace.
Attrezzature
Becco Bunsen
Filo di platino o di nichel-cromo fissato su apposito supporto o su bacchetta di vetro
Vetrini da orologio contenenti le sostanze da analizzare
Materiali e reagenti
Borace
Cloruri di cobalto, cromo, manganese, rame, ferro e nichel.
Procedimento
Arroventare la punta di un filo di platino (o di nichel-cromo) e prelevare la polvere di borace. Riportare nuovamente il filo alla fiamma del Bunsen sino a quando non si ottiene una massa vetrosa (perla). Ripetere tale operazione finché si ottiene una perla con un diametro di 1,5-2 mm.
Arroventare la perla e fare aderire ad essa una piccola quantità della sostanza da analizzare.
Riportare la perla alla fiamma del Bunsen sino a quando diventa trasparente.
Osservare la colorazione assunta dalla perla sia a caldo che a freddo.
Ruotare il manicotto presente alla base del cannello del Bunsen in modo da diminuire la quantità di aria aspirata e rendere quindi la fiamma riducente (fiamma di colore giallo).
Portare nuovamente la perla alla fiamma del Bunsen.
Osservare la nuova colorazione assunta dalla perla.
Ripetere tali operazioni per tutte le sostanza da analizzare.

Tipologie di fiamma del Becco Bunsen. A sinistra fimma riducente. A destra fiamma ossidante.
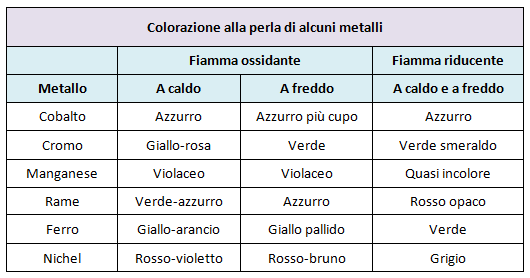
Confronto dei diversi colori assunti dalla perla.
Conclusioni
Il saggio alla perla al borace è un saggio per via secca utile per l'identificazione dei composti di alcuni metalli; è un saggio alternativo o complemenare ai saggi alla fiamma.
Operando con fiamma ossidante, i cloruri dei metalli vengono convertiti nei corrispondenti ossidi.
L'anidride borica ottenuta per riscaldamento alla fiamma del borace coverte tali ossidi in metaborati che assumono colori caratteristici a seconda del metallo che contengono. Un esempio di reazione è la seguente:
![]()
In tale reazione si forma il metaborato rameico di colore azzurro.
Operando con fiamma riducente, ovvero in presenza di polvere di carbone incombusta, il metaborato si riduce dando una perla di colore diverso.
Studia con noi